بخش ۱: تحولات نوین در درمان سکته مغزی ایسکمیک
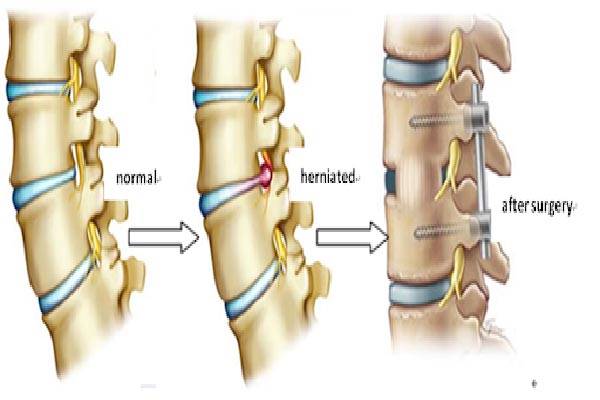
درمان سکته مغزی ایسکمیک، که ناشی از انسداد یک رگ خونی در مغز است، در دهه گذشته شاهد یک انقلاب واقعی بوده است. رویکرد درمانی از یک پارادایم سفت و سخت مبتنی بر «زمان» به یک نگرش فردیسازیشده و مبتنی بر «بافت مغزی قابل نجات» تغییر یافته است. این تحول، که با پیشرفتهای چشمگیر در داروها و تکنیکهای مداخلهای همراه بوده، افقهای جدیدی را برای بهبود نتایج بیماران گشوده است.
۱.۱ درمانهای حلکننده لخته (ترومبولیز): فراتر از استاندارد طلایی
برای بیش از دو دهه، داروی «آلتپلاز» (Alteplase یا rtPA) استاندارد طلایی درمان ترومبولیتیک برای حل کردن لخته خون در ساعات اولیه سکته مغزی بوده است. این دارو باید در یک پنجره زمانی محدود (معمولاً ۳ تا ۴.۵ ساعت پس از شروع علائم) و از طریق یک پروتکل تزریق نسبتاً پیچیده (یک دوز اولیه سریع و سپس انفوزیون طی یک ساعت) تجویز شود. با وجود اثربخشی، این محدودیتها همواره چالشهایی را در مدیریت سریع بیماران ایجاد کردهاند.
معرفی داروی تنکتپلاز (Tenecteplase – TNK): نسل جدید درمان
اخیراً، داروی «تنکتپلاز» (Tenecteplase) به عنوان یک جایگزین قدرتمند و بسیار کاربردیتر برای آلتپلاز مطرح شده است. بزرگترین مزیت تنکتپلاز، نحوه تجویز آن است: یک تزریق سریع و تکمرحلهای وریدی (بولوس) که طی چند ثانیه انجام میشود. این ویژگی به ظاهر ساده، پیامدهای عملی بسیار مهمی دارد:
- سرعت و سهولت: حذف نیاز به انفوزیون یک ساعته، فرآیند درمان را به شدت تسریع میکند، خطاهای احتمالی در دوزبندی را کاهش میدهد و تیم درمانی را برای انجام اقدامات بعدی (مانند آمادهسازی بیمار برای انتقال به بخش آنژیوگرافی) آزاد میگذارد.
- شواهد بالینی: کارآزماییهای بالینی بزرگ و معتبری مانند کارآزمایی AcT در سال ۲۰۲۲ نشان دادند که تنکتپلاز با دوز 0.25 mg/kg (حداکثر ۲۵ میلیگرم) از نظر نتایج عملکردی در ۹۰ روز پس از سکته، ضعیفتر از آلتپلاز نیست و جایگاه خود را به عنوان یک جایگزین منطقی تثبیت کرده است. علاوه بر این، متاآنالیزها و مطالعاتی مانند EXTEND-IA TNK نشان دادهاند که تنکتپلاز در باز کردن عروق بزرگ مغزی (LVO) و بهبود اولیه عصبی حتی ممکن است برتریهایی نیز داشته باشد.
این سهولت در استفاده، تنکتپلاز را به گزینهای ایدهآل برای مدلهای درمانی نوین مانند «واحدهای سیار سکته مغزی» (Mobile Stroke Units) و سیستم «Drip-and-Ship» تبدیل کرده است. در این سیستم، بیمار در یک بیمارستان کوچکتر و فاقد امکانات پیشرفته، درمان اولیه ترومبولیتیک را به سرعت دریافت کرده و سپس برای اقدامات تخصصیتر مانند ترومبکتومی مکانیکی به یک مرکز جامع سکته مغزی منتقل میشود. تزریق سریع تنکتپلاز این فرآیند انتقال را بسیار سادهتر و ایمنتر میکند. به نوعی، تنکتپلاز در حال «دموکراتیزه کردن» درمان سریع سکته مغزی است و به کاهش نابرابری در دسترسی به مراقبتهای حیاتی بین مراکز شهری بزرگ و مناطق دورافتاده کمک میکند.
۱.۲ ترومبکتومی مکانیکی (Endovascular Thrombectomy – EVT): انقلابی در درمان سکتههای شدید
ترومبکتومی مکانیکی یک روش کمتهاجمی و فوق تخصصی است که مسیر درمان سکتههای مغزی شدید ناشی از انسداد عروق بزرگ (LVO) را به کلی دگرگون کرده است. در این روش، یک متخصص نورواینترونشنال (فوق تخصص مغز و اعصاب مداخلهای) یک کاتتر بسیار نازک را از طریق شریانی در کشاله ران یا مچ دست، به سمت رگ مسدود شده در مغز هدایت میکند. سپس با استفاده از ابزارهای خاصی مانند «استنت رتریور» (یک توری فلزی بازشونده) یا کاتتر آسپیراسیون (مکنده)، لخته خون را به صورت فیزیکی گرفته و از رگ خارج میکند.
اثربخشی این روش به قدری چشمگیر است که یکی از موفقترین مداخلات در تاریخ پزشکی مدرن محسوب میشود. متاآنالیز بزرگ HERMES در سال ۲۰۱۵ به طور قطعی نشان داد که ترومبکتومی در بیماران منتخب، نتایج عملکردی را به شکل چشمگیری بهبود میبخشد. «عدد مورد نیاز برای درمان» (NNT) برای رسیدن به استقلال عملکردی در این روش بین ۳ تا ۷ است؛ این یعنی به ازای هر ۳ تا ۷ بیماری که تحت درمان قرار میگیرند، یک نفر از ناتوانی شدید نجات پیدا میکند.
گسترش پنجره زمانی درمان (تا ۲۴ ساعت)
در ابتدا، ترومبکتومی فقط برای بیمارانی که در ۶ ساعت اول پس از شروع علائم مراجعه میکردند، انجام میشد. اما دو کارآزمایی بالینی تاریخساز به نامهای DAWN و DEFUSE-3 این محدودیت را شکستند. این مطالعات نشان دادند که با استفاده از تصویربرداری پیشرفته مغز، میتوان بیمارانی را که حتی تا ۲۴ ساعت پس از شروع علائم، همچنان بافت مغزی قابل نجات (پنومبرا) دارند، شناسایی و با موفقیت درمان کرد. این پیشرفت یک موهبت بزرگ برای بیمارانی است که با «سکته در خواب» (Wake-up Stroke) مواجه میشوند یا به دلایل مختلف دیر به بیمارستان میرسند.
۱.۳ نقش تصویربرداری پیشرفته: گذار از پارادایم «زمان» به «بافت»
موفقیتهای اخیر در درمان سکته مغزی ایسکمیک، مدیون تغییر نگرش از «زمان» به «بافت» است. دیگر تنها سوال این نیست که «چقدر از شروع علائم گذشته است؟»، بلکه سوال مهمتر این است که «چه مقدار از بافت مغز قابل نجات است؟». ابزارهای کلیدی در این ارزیابی عبارتند از:
- CT پرفیوژن (CTP) و MRI پیشرفته (DWI/FLAIR Mismatch): این تکنیکها میتوانند با دقت بالایی بین «هسته ایسکمیک» (بافت مغزی که به طور غیرقابل برگشت آسیب دیده) و «پنومبرا» (بافت در معرض خطری که با بازگشایی رگ قابل نجات است) تمایز قائل شوند. وجود یک عدم تطابق بزرگ بین هسته کوچک و پنومبرای بزرگ، نشاندهنده پتانسیل بالای بهبودی با درمانهای بازکننده عروق است، حتی اگر ساعتها از شروع سکته گذشته باشد.
- CT آنژیوگرافی (CTA): این روش به سرعت و با دقت بالا، وجود انسداد در عروق بزرگ مغزی را نشان میدهد و به تیم درمانی کمک میکند تا در چند دقیقه برای انجام ترومبکتومی مکانیکی تصمیمگیری کنند.
با این حال، موفقیت چشمگیر ترومبکتومی مکانیکی، یک چالش جدید و بزرگ را در سیستمهای بهداشتی ایجاد کرده است: چالش دسترسی و عدالت. این روش نیازمند تیمهای فوق تخصصی، تجهیزات گرانقیمت و زیرساختهای پیچیده است که تنها در مراکز جامع سکته مغزی یافت میشود. مطالعات نشان میدهند که بیماران، به ویژه در مناطق روستایی و دورافتاده، که ابتدا به بیمارستانهای کوچکتر مراجعه میکنند، شانس بسیار کمتری برای دریافت این درمان حیاتی دارند. بنابراین، امروزه گلوگاه اصلی در بهبود نتایج سکتههای شدید، دیگر صرفاً یک مسئله پزشکی نیست، بلکه یک چالش لجستیکی، زیرساختی و مرتبط با سیاستگذاریهای بهداشت عمومی است. آینده درمان سکته مغزی LVO، به همان اندازه که به نوآوری در ابزارهای پزشکی وابسته است، به بهینهسازی پروتکلهای اورژانس پیشبیمارستانی، ایجاد شبکههای منطقهای ارجاع بیمار و استفاده از فناوریهایی مانند هوش مصنوعی برای تسریع فرآیندها بستگی دارد.
| ویژگی | آلتپلاز (Alteplase) | تنکتپلاز (Tenecteplase) |
| نحوه تزریق | تزریق بولوس وریدی و سپس انفوزیون ۶۰ دقیقهای | تزریق تکمرحلهای بولوس وریدی طی ۵-۱۰ ثانیه |
| دوزبندی | 0.9 mg/kg (حداکثر ۹۰ میلیگرم) | 0.25 mg/kg (حداکثر ۲۵ میلیگرم) |
| ویژگی در اتصال به فیبرین | پایینتر | بالاتر |
| کارآزماییهای کلیدی | NINDS, ECASS-III | AcT, EXTEND-IA TNK, NOR-TEST |
| مزیت اصلی | استاندارد درمانی تثبیتشده با سابقه طولانی | سرعت و سهولت فوقالعاده در تزریق |
بخش ۲: افقهای جدید در مدیریت سکته مغزی هموراژیک
سکته مغزی هموراژیک (خونریزیدهنده)، که در اثر پاره شدن یک رگ خونی در مغز رخ میدهد، همواره یکی از مرگبارترین انواع سکته بوده و گزینههای درمانی مؤثر برای آن بسیار محدود بوده است. برای دههها، مدیریت این بیماران عمدتاً بر مراقبتهای حمایتی مانند کنترل فشار خون و مدیریت تورم مغز متمرکز بود. اما اکنون، با ظهور تکنیکهای جراحی نوین و تحقیقات پیشگامانه در حوزه پزشکی بازساختی، این چشمانداز در حال تغییر است.
۲.۱ جراحی کمتهاجمی (Minimally Invasive Surgery – MIS): تخلیه هماتوم با حداقل آسیب
جراحی سنتی برای تخلیه لخته خون (هماتوم) از مغز، یعنی کرانیوتومی باز، در کارآزماییهای بزرگ نتوانسته است به طور مداوم برتری خود را نسبت به درمانهای غیرجراحی نشان دهد. این امر محققان را به سمت توسعه روشهای کمتهاجمی سوق داده است که هدفشان تخلیه هماتوم با کمترین آسیب ممکن به بافت سالم مغز است. این تکنیکها معمولاً با استفاده از سیستمهای ناوبری استریوتاکتیک (مشابه GPS برای مغز) انجام میشوند تا دقت به حداکثر برسد. دو رویکرد اصلی عبارتند از:
- تخلیه آندوسکوپیک: در این روش، جراح از طریق یک سوراخ بسیار کوچک در جمجمه، یک لوله نازک مجهز به دوربین و ابزار (آندوسکوپ) را به داخل هماتوم هدایت میکند. این کار به جراح اجازه میدهد تا لخته را به صورت زنده مشاهده کرده و با استفاده از ابزارهای مخصوص آن را با دقت تخلیه کند.
- آسپیراسیون استریوتاکتیک همراه با ترومبولیز (روش MISTIE): در این تکنیک، یک کاتتر نازک با هدایت تصویربرداری در مرکز هماتوم قرار داده میشود. سپس، مقدار کمی داروی حلکننده لخته (مانند آلتپلاز) به داخل لخته تزریق میشود تا آن را مایع کند. در نهایت، لخته مایع شده به آرامی طی چند روز از طریق کاتتر تخلیه میشود. اگرچه کارآزمایی MISTIE-III نتوانست به هدف اصلی خود یعنی بهبود عملکردی بیماران دست یابد، اما تحلیلهای بعدی نشان داد که این روش میتواند به کاهش مرگومیر کمک کند.
شواهد جدیدتر، به ویژه از کارآزماییهایی مانند ENRICH، نشان میدهند که جراحی کمتهاجمی، به شرطی که در زمان مناسب (معمولاً طی ۲۴ ساعت اول) و در بیماران منتخب انجام شود، میتواند به بهبود نتایج عملکردی و کاهش مرگومیر منجر شود. این رویکردها نمایانگر یک تغییر پارادایم اساسی در درمان سکته هموراژیک هستند: گذار از یک استراتژی منفعلانه «کنترل آسیب» به یک استراتژی فعالانه «ترمیم و پاکسازی». این نگرش جدید، هماتوم را نه فقط یک توده فضاگیر، بلکه یک منبع سمی و فعال از آسیبهای ثانویه به مغز میداند که حذف سریع آن میتواند کلید بهبود نتایج باشد.
۲.۲ درمانهای نوظهور و تحقیقاتی در خط مقدم علم
افقهای درمانی سکته هموراژیک فراتر از تکنیکهای جراحی رفته و به حوزه پزشکی مولکولی و فناوریهای پیشرفته نیز کشیده شده است.
- سلولهای بنیادی (Stem Cell Therapy): پتانسیل ترمیم عصبیتحقیقات پیشگامانه در مراکزی مانند مایو کلینیک، در حال بررسی استفاده از سلولهای بنیادی مزانشیمی برای درمان سکته هموراژیک است. نکته جالب این است که این سلولها احتمالاً جایگزین سلولهای عصبی مرده نمیشوند، بلکه مانند «کارخانههای داروسازی مینیاتوری» عمل میکنند. آنها با ترشح فاکتورهای ضدالتهابی و محافظتکننده عصبی (مانند اینترلوکین-۶ و VEGF)، به نجات نورونهای آسیبدیده در اطراف ناحیه خونریزی کمک کرده و فرآیندهای ترمیمی مغز را تقویت میکنند. در مطالعات پیشبالینی، مشخص شد که تزریق وریدی این سلولها مؤثرتر از تزریق مستقیم به مغز است، که نشان میدهد این سلولها میتوانند از راه دور و با عبور از سد خونی-مغزی، اثرات درمانی خود را اعمال کنند. اگرچه این تحقیقات هنوز در مراحل اولیه (فاز ۱ کارآزمایی بالینی) قرار دارد، اما برای اولین بار امیدی برای «ترمیم عصبی» واقعی در بیماران سکته هموراژیک ایجاد کرده است.
- هوش مصنوعی (Artificial Intelligence – AI): تسریع در تشخیص و درماندر سکته هموراژیک، هر دقیقه اهمیت دارد؛ تخمین زده میشود که در دو ساعت اول، بیماران در هر دقیقه بین ۶ تا ۸ میلیون سلول مغزی از دست میدهند. هوش مصنوعی در حال تبدیل شدن به یک ابزار قدرتمند برای فشردهسازی این زمان حیاتی است. الگوریتمهای AI میتوانند صدها تصویر سیتی اسکن مغز را در عرض چند ثانیه تحلیل کرده، محل دقیق خونریزی را مشخص کنند و به طور خودکار به تیم سکته مغزی هشدار دهند. این فرآیند که به صورت دستی ممکن است تا ۳۰ دقیقه طول بکشد، با کمک AI به چند ثانیه کاهش مییابد. این صرفهجویی در زمان میتواند تأثیر شگرفی بر نتایج بیمار داشته باشد و تعداد بسیار زیادی از نورونها را از مرگ حتمی نجات دهد.
این پیشرفتهای فناورانه، علاوه بر پتانسیل درمانی، چالشهای جدیدی را نیز به همراه دارند. توسعه سیستمهای جراحی کمتهاجمی که استفاده از آنها سادهتر است، این سوال را مطرح کرده که آیا متخصصان دیگری غیر از جراحان مغز و اعصاب (مانند نورواینترونشنالیستها) نیز میتوانند این процедуры را انجام دهند؟ این موضوع یک بحث جدی بین انجمنهای تخصصی ایجاد کرده است؛ از یک سو، نیاز به افزایش دسترسی بیماران به این درمانهای حیاتی و از سوی دیگر، ضرورت حفظ بالاترین استانداردهای ایمنی و مهارت. حل این چالش نیازمند بازنگری در پروتکلهای آموزشی و صدور گواهینامههای تخصصی در آینده خواهد بود.
بخش ۳: پیشگیری از سکته مغزی: راهنمای جامع مبتنی بر شواهد جدید
بهترین راه مقابله با سکته مغزی، پیشگیری از وقوع آن است. خبر خوب این است که با مدیریت هوشمندانه عوامل خطر و اتخاذ یک سبک زندگی سالم، میتوان از وقوع بیش از ۸۰٪ سکتههای مغزی جلوگیری کرد. علم پیشگیری از سکته مغزی در سالهای اخیر پیشرفتهای قابل توجهی داشته و اهداف درمانی برای کنترل عوامل خطر، سختگیرانهتر و دقیقتر شدهاند.
۳.۱ مدیریت هوشمندانه عوامل خطر اصلی
مدیریت سه عامل خطر کلیدی—فشار خون، کلسترول و دیابت—سنگ بنای پیشگیری از سکته مغزی است.
- کنترل فشار خون (Hypertension): فشار خون بالا مهمترین عامل خطر قابل اصلاح برای هر دو نوع سکته مغزی ایسکمیک و هموراژیک است. دستورالعملهای جدید، اهداف درمانی سختگیرانهتری را توصیه میکنند. برای بیمارانی که سابقه سکته مغزی یا حمله ایسکمیک گذرا (TIA) داشتهاند، هدف درمانی، رساندن فشار خون به زیر 130/80 mmHg است. این هدف نسبت به توصیههای قبلی (<140/90 mmHg) تهاجمیتر است و بر اساس شواهد محکمی استوار است که نشان میدهد کنترل شدیدتر فشار خون، خطر سکته مغزی مجدد را بیشتر کاهش میدهد.
- مدیریت کلسترول (Dyslipidemia): کلسترول بالا، به ویژه کلسترول بد (LDL)، با ایجاد پلاکهای آترواسکلروتیک در دیواره عروق، زمینهساز سکته مغزی ایسکمیک میشود.
- نقش حیاتی استاتینها: درمان با داروهای استاتین با شدت بالا (High-intensity statin therapy) برای اکثر بیمارانی که دچار سکته مغزی با منشأ آترواسکلروز شدهاند، ضروری است.
- اهداف درمانی LDL: بر اساس نتایج کارآزماییهای بزرگ، هدف درمانی برای کلسترول LDL در این بیماران، رساندن آن به زیر 70 mg/dL است. اصل راهنما در مدیریت کلسترول، «هرچه پایینتر، بهتر» است. اگر با حداکثر دوز قابل تحمل استاتین به این هدف نرسیم، افزودن داروهای دیگری مانند «ازتیمایب» (Ezetimibe) توصیه میشود.
- کنترل دیابت (Diabetes): دیابت خطر سکته مغزی را بیش از دو برابر افزایش میدهد. مدیریت دیابت فراتر از کنترل صرف قند خون است.
- داروهای نوین با مزایای قلبی-عروقی: دستورالعملهای جدید تأکید دارند که برای بیماران دیابتی با سابقه بیماریهای قلبی-عروقی، باید از داروهایی استفاده کرد که اثرات محافظتی اثباتشدهای بر روی قلب و عروق دارند. دو دسته دارویی آگونیستهای گیرنده GLP-1 و مهارکنندههای SGLT2 نشان دادهاند که میتوانند خطر حوادث قلبی-عروقی، از جمله سکته مغزی را کاهش دهند و باید به عنوان بخشی از رژیم درمانی این بیماران در نظر گرفته شوند.
یک مفهوم کلیدی در پیشگیری مدرن، قدرت «اثر تجمعی» است. مطالعات نشان دادهاند که ترکیبی از اقدامات—مصرف آسپرین، استاتین، و داروهای ضد فشار خون، همراه با اصلاح رژیم غذایی و ورزش—میتواند خطر حوادث عروقی مجدد را تا ۸۰٪ کاهش دهد. این پیام بسیار قدرتمندی است: با تمرکز بر مدیریت چند عامل کلیدی، میتوان به طور چشمگیری از خود در برابر این بیماری ویرانگر محافظت کرد.
۳.۲ سبک زندگی به عنوان یک سپر دفاعی قدرتمند
داروها به تنهایی کافی نیستند. انتخابهای روزمره ما در سبک زندگی، نقشی حیاتی و غیرقابل انکار در پیشگیری از سکته مغزی دارند.
- تغذیه: دو الگوی غذایی به طور خاص برای سلامت قلب و عروق و پیشگیری از سکته مغزی توصیه میشوند:
- رژیم مدیترانهای: این رژیم سرشار از میوهها، سبزیجات، غلات کامل، حبوبات، آجیل و روغن زیتون است و مصرف گوشت قرمز و چربیهای اشباع در آن محدود است.
- رژیم DASH: این رژیم که برای کنترل فشار خون طراحی شده، بر مصرف میوهها، سبزیجات و لبنیات کمچرب تأکید دارد و میزان سدیم (نمک) در آن بسیار پایین است.
- فعالیت بدنی: بیتحرکی یک عامل خطر مستقل برای سکته مغزی است. توصیه میشود بزرگسالان حداقل ۱۵۰ دقیقه فعالیت هوازی با شدت متوسط (مانند پیادهروی سریع) یا ۷۵ دقیقه فعالیت با شدت بالا (مانند دویدن) در هفته داشته باشند.
- ترک سیگار و الکل: سیگار کشیدن با آسیب رساندن به دیواره رگهای خونی، خطر سکته مغزی را به شدت افزایش میدهد. ترک کامل سیگار یکی از مؤثرترین اقدامات پیشگیرانه است. مصرف الکل نیز باید به حداقل ممکن محدود شود.
- کنترل وزن: چاقی و اضافه وزن با افزایش فشار خون، کلسترول و خطر دیابت، به طور غیرمستقیم احتمال وقوع سکته مغزی را بالا میبرند. حفظ وزن سالم از طریق رژیم غذایی متعادل و فعالیت بدنی منظم، یک جزء اساسی در برنامه پیشگیری است.
| توصیه | هدف | جزئیات کلیدی |
| رژیم غذایی | سبک مدیترانهای یا DASH | تاکید بر میوه، سبزیجات، آجیل، غلات کامل؛ کاهش سدیم و چربیهای اشباع |
| فعالیت بدنی | ۱۵۰ دقیقه متوسط یا ۷۵ دقیقه شدید در هفته | ورزشهای هوازی مانند پیادهروی سریع، شنا، دوچرخهسواری |
| فشار خون | <130/80 mmHg | کنترل منظم، پایبندی به دارو، رژیم کمنمک |
| کلسترول (LDL) | <70 mg/dL (برای بیماران پرخطر) | درمان با استاتین، رژیم کمچربی اشباع |
| وزن | BMI 18.5−24.9 kg/m2 | تعادل کالری دریافتی و مصرفی از طریق رژیم و ورزش |
| سیگار | ترک کامل | دریافت حمایت پزشکی و اجتماعی برای موفقیت در ترک |
بخش ۴: توانبخشی پس از سکته مغزی: بازگشت به زندگی با فناوریهای نوین
تا همین اواخر، پیشرفتها در حوزه توانبخشی پس از سکته مغزی از پیشرفتهای چشمگیر در درمان حاد آن عقب مانده بود. تمرکز اصلی توانبخشی بر آموزش راهکارهای «جبرانی» بود؛ یعنی به بیمار کمک میشد تا با استفاده از اعضای سالم بدن، محدودیتهای ناشی از سکته را جبران کند. اما امروزه، با ظهور فناوریهای نوین، پارادایم توانبخشی در حال یک تغییر بنیادی است: از جبران به سمت ترمیم و بازیابی. هدف جدید، تحریک فعالانه مغز برای بازسازی مسیرهای عصبی آسیبدیده و بازگرداندن هرچه بیشتر عملکرد به اندامهای فلج شده است.
۴.۱ تحریک عصبی برای بهبود عملکرد حرکتی
این روشها با استفاده از پالسهای الکتریکی یا مغناطیسی، فعالیت نواحی خاصی از مغز را تعدیل میکنند تا پدیده «نوروپلاستیسیتی» (قابلیت مغز برای بازآرایی خود) را تقویت کنند.
- تحریک عصب واگ (Vagus Nerve Stimulation – VNS): این یک فناوری پیشگامانه و تأیید شده توسط FDA است که به طور خاص برای بهبود عملکرد حرکتی دست و بازو طراحی شده است. در این روش، یک دستگاه کوچک شبیه به ضربانساز قلب، زیر پوست قفسه سینه کاشته میشود و یک سیم نازک از آن به عصب واگ در گردن متصل میگردد. نکته کلیدی این است که دستگاه، پالسهای الکتریکی خفیفی را دقیقاً در حین انجام تمرینات توانبخشی توسط بیمار ارسال میکند. این «تحریک زوجشده» (Paired Stimulation) مغز را «آماده» میکند تا اثرات تمرینات فیزیکی چندین برابر شود و به بازسازی مدارهای عصبی کمک کند. مطالعات بالینی نشان دادهاند که VNS میتواند ماهها یا حتی سالها پس از سکته، بهبودی قابل توجهی در قدرت و عملکرد حرکتی اندام فوقانی ایجاد کند.
- سایر تکنیکهای تحریک مغز: روشهای غیرتهاجمی مانند تحریک مغناطیسی ترانسکرانیال (TMS) و تحریک الکتریکی مستقیم ترانسکرانیال (tDCS) نیز در حال تحقیق و توسعه هستند. این تکنیکها بدون نیاز به جراحی و با قرار دادن دستگاههایی بر روی پوست سر، فعالیت مغز را برای تقویت بهبودی در حوزههای حرکتی و گفتاری تعدیل میکنند.
این رویکردها نشان میدهند که بهبودی پس از سکته مغزی یک فرآیند ایستا نیست که پس از چند ماه متوقف شود. با تحریک مناسب، مغز پتانسیل ترمیم و یادگیری مجدد را برای مدت طولانی حفظ میکند. فناوریهای نوین در حال تبدیل شدن به کلیدی برای گشودن این پتانسیل هستند و یک همافزایی قدرتمند بین فناوری و توانبخشی سنتی ایجاد میکنند؛ جایی که هر یک، اثر دیگری را تقویت میکند.
۴.۲ ابزارهای فناورانه در توانبخشی مدرن
فناوریهای دیجیتال در حال متحول کردن نحوه ارائه و دریافت خدمات توانبخشی هستند.
- رباتیک و اسکلتهای بیرونی (Robotics and Exoskeletons): دستگاههای رباتیک میتوانند به بیماران کمک کنند تا تمرینات تکراری و هدفمند را با شدت و دقتی بسیار بالاتر از توانبخشی سنتی انجام دهند. یک بازوی رباتیک میتواند اندام ضعیف بیمار را حمایت کرده، آن را در مسیر صحیح حرکت هدایت کند و بازخورد دقیقی در مورد عملکرد بیمار ارائه دهد. این «تمرین با تکرار بالا» برای تحریک نوروپلاستیسیتی ضروری است.
- واقعیت مجازی (VR) و واقعیت افزوده (AR): این فناوریها با ایجاد محیطهای مجازی جذاب و تعاملی، فرآیند توانبخشی را به یک «بازی» تبدیل میکنند. این «گیمیفیکیشن» انگیزه و پایبندی بیماران به برنامههای تمرینی خستهکننده را به شدت افزایش میدهد. بیمار میتواند در یک محیط امن مجازی، فعالیتهای روزمره مانند خرید کردن یا آشپزی را تمرین کند و به تدریج مهارتهای خود را بازیابد.
- توانبخشی از راه دور (Telerehabilitation) و حسگرهای پوشیدنی: این حوزه به سرعت در حال رشد است و به بیماران اجازه میدهد تا خدمات توانبخشی با کیفیت بالا را در منزل خود دریافت کنند. از طریق ویدئو کنفرانس، اپلیکیشنهای موبایل و حسگرهای پوشیدنی (که حرکات بیمار را ردیابی میکنند)، درمانگر میتواند از راه دور بر تمرینات بیمار نظارت کرده، بازخورد ارائه دهد و برنامه درمانی را تنظیم کند. این رویکرد نه تنها هزینهها را کاهش میدهد و مشکلات حمل و نقل را برطرف میکند، بلکه به بیمار قدرت میدهد تا نقش فعالتری در فرآیند بهبودی خود ایفا کند.
بخش ۵: ملاحظات ویژه در سکته مغزی
سکته مغزی یک بیماری یکسان برای همه نیست. عوامل مختلفی مانند سن، جنسیت و شرایط پزشکی زمینهای میتوانند بر عوامل خطر، علائم و نتایج بیماری تأثیر بگذارند. درک این تفاوتها برای تشخیص به موقع، پیشگیری مؤثر و درمان مناسب ضروری است.
۵.۱ سکته مغزی در جوانان: یک تهدید رو به رشد
برخلاف تصور عمومی که سکته مغزی را بیماری سالمندان میداند، شیوع آن در جوانان و افراد میانسال (سنین ۱۵ تا ۴۹ سال) به طرز نگرانکنندهای در حال افزایش است. تخمین زده میشود که اکنون از هر ۷ مورد سکته مغزی، یک مورد در این گروه سنی رخ میدهد. این افزایش تا حدی به دلیل شیوع بیشتر عوامل خطر سنتی مانند چاقی، فشار خون بالا و دیابت در سنین پایینتر است. اما سکته مغزی در جوانان دارای عوامل خطر منحصر به فردی نیز هست که اغلب نادیده گرفته میشوند:
- دایسکشن شریانی (Arterial Dissection): یکی از شایعترین علل سکته مغزی در افراد زیر ۴۵ سال، پارگی لایههای داخلی دیواره شریانهای گردن (کاروتید یا ورتبرال) است. این پارگی میتواند منجر به تشکیل لخته و انسداد رگ شود.
- بیماریهای قلبی مادرزادی: وجود یک سوراخ کوچک در دیواره بین دو دهلیز قلب به نام «فورامن اوال باز» (PFO) که در حدود ۲۵٪ از جمعیت عمومی وجود دارد، میتواند باعث عبور لختههای خون از سمت راست به چپ قلب و رسیدن آنها به مغز شود. این عامل، علت بسیاری از سکتههای مغزی با منشأ نامشخص در جوانان است.
- اختلالات انعقادی (Hypercoagulable States): برخی بیماریهای ارثی یا اکتسابی مانند «سندرم آنتیفسفولیپید» باعث میشوند خون راحتتر لخته شود و خطر سکته مغزی را افزایش میدهند.
- میگرن همراه با اورا (Migraine with Aura): این نوع خاص از میگرن، به ویژه در زنان جوانی که سیگار میکشند یا از قرصهای ضدبارداری استروژندار استفاده میکنند، خطر سکته مغزی ایسکمیک را به طور قابل توجهی افزایش میدهد.
۵.۲ تفاوتهای جنسیتی در سکته مغزی: چرا زنان متفاوت هستند؟
سکته مغزی در زنان و مردان تفاوتهای مهمی دارد. اگرچه بروز سکته مغزی در سنین مشابه در مردان بیشتر است، اما از آنجایی که زنان عمر طولانیتری دارند، در مجموع تعداد بیشتری از زنان دچار سکته مغزی میشوند و مرگومیر ناشی از آن نیز در آنها بالاتر است.
علائم غیرمعمول و منتشر: یک بحران تشخیص نادرست
مهمترین تفاوت، در علائم بیماری نهفته است. در حالی که مردان بیشتر علائم کلاسیک سکته مغزی (ضعف ناگهانی یک طرف بدن، اختلال در تکلم، افتادگی صورت) را تجربه میکنند، زنان به احتمال بیشتری علائم «غیرمعمول» یا «منتشر» را گزارش میدهند. این علائم عبارتند از:
- ضعف عمومی و ناگهانی
- خستگی شدید و بیدلیل
- گیجی یا تغییر در وضعیت ذهنی
- حالت تهوع
- درد قفسه سینه یا تپش قلب
- سکسکه
این علائم مبهم به راحتی میتوانند با بیماریهای دیگر اشتباه گرفته شوند یا توسط خود بیمار و حتی کادر درمان جدی گرفته نشوند. این «سوءتعبیر بزرگ» منجر به تأخیر حیاتی در مراجعه به اورژانس و شروع درمان میشود. از آنجایی که در درمان سکته مغزی «زمان طلاست»، این تأخیر به طور مستقیم به نتایج بدتر، ناتوانی بیشتر و مرگومیر بالاتر در زنان منجر میشود. بنابراین، آموزش عمومی باید فراتر از علائم کلاسیک رفته و بر این علائم غیرمعمول در زنان نیز تأکید کند.
عوامل خطر مختص زنان:
علاوه بر عوامل خطر مشترک، زنان دارای ریسک فاکتورهای منحصر به فردی هستند:
- بارداری و دوره پس از زایمان: خطر سکته مغزی در این دوران افزایش مییابد.
- پرهاکلامپسی: سابقه فشار خون بالای بارداری، خطر سکته مغزی در آینده را دو برابر میکند.
- قرصهای ضدبارداری: قرصهای حاوی استروژن میتوانند خطر سکته را، به ویژه در صورت همراهی با سیگار یا میگرن، افزایش دهند.
- فیبریلاسیون دهلیزی (AFib): این آریتمی قلبی شایع، در زنان با احتمال بیشتری منجر به سکته مغزی شدید میشود.
۵.۳ کووید-۱۹ و سکته مغزی: ارتباط پنهان
پاندمی کووید-۱۹ نشان داد که عفونت SARS-CoV-2 تنها یک بیماری تنفسی نیست، بلکه میتواند عوارض جدی عروقی، از جمله سکته مغزی، ایجاد کند. این ویروس از چندین مسیر خطر سکته را افزایش میدهد:
- حالت انعقادپذیری بالا (Hypercoagulable State): ویروس یک پاسخ التهابی شدید در بدن ایجاد میکند که به آن «طوفان سیتوکینی» میگویند. این التهاب گسترده، سیستم انعقاد خون را بیش از حد فعال کرده و منجر به تشکیل لختههای متعدد در سراسر بدن، از جمله در عروق مغزی میشود.
- آسیب به دیواره عروق (Endothelial Injury): ویروس میتواند مستقیماً به سلولهای پوشاننده دیواره داخلی رگهای خونی (اندوتلیوم) حمله کرده و به آنها آسیب برساند. این آسیب، زمینه را برای تشکیل لخته و بیثبات شدن پلاکهای آترواسکلروتیک موجود فراهم میکند.
- اختلال در تنظیم فشار خون: ویروس SARS-CoV-2 برای ورود به سلولها از گیرندهای به نام ACE2 استفاده میکند. این گیرنده نقش مهمی در تنظیم فشار خون دارد. اشغال و تخریب این گیرندهها توسط ویروس میتواند سیستم تنظیم فشار خون را مختل کرده و با افزایش ناگهانی فشار خون، خطر سکته مغزی هموراژیک را بالا ببرد.